
Permanganat Formülü Nedir?
Permanganat, potasyum permanganat formülü ile bilinen, güçlü bir oksidan olan bir kimyasal bileşiktir. Su arıtımı, dezenfeksiyon ve laboratuvar uygulamalarında yaygın olarak kullanılır. Kimyasal tepkimelerde önemli bir rol oynar ve kullanımı sırasında güvenlik önlemleri alınması gereklidir.
Permanganat Nedir?Permanganat, kimyada genellikle potasyum permanganat (KMnO₄) formülü ile bilinen bir bileşiktir. Permanganat iyonu (MnO₄⁻), güçlü bir oksidandır ve birçok kimyasal reaksiyonda kullanılır. Potasyum permanganat, su arıtımında, dezenfeksiyonda ve laboratuvar uygulamalarında yaygın olarak kullanılmaktadır. Bu bileşik, derin mor rengi ile tanınır ve suda çözündüğünde mor bir solüsyon oluşturur. Permanganatın Kimyasal Özellikleri Permanganat, oldukça reaktif bir bileşiktir ve birçok farklı ortamda çeşitli reaksiyonlar gerçekleştirebilir. Aşağıda permanganatın kimyasal özelliklerine dair bazı önemli noktalar bulunmaktadır:
Permanganatın Kullanım Alanları Permanganatın çeşitli endüstrilerde ve bilimsel uygulamalarda birçok kullanımı bulunmaktadır:
Permanganatın Oluşumu ve Reaksiyonları Permanganat, genellikle mangan oksit (MnO₂) veya mangan karbür (Mn₃C) gibi mangan bileşiklerinin oksitlenmesi ile elde edilir. Ayrıca, permanganatın redoks reaksiyonları sırasında çeşitli ürünler oluşturması mümkündür. Örneğin, asidik bir ortamda permanganatın potasyum klorür (KCl) ile tepkime vermesi sonucunda klor gazı ve mangan(II) klorür (MnCl₂) oluşur. Güvenlik ve Riskler Permanganat, yüksek oksidatif özellikleri nedeniyle dikkatli kullanılmalıdır. Cilt ile teması, yanıklara neden olabilir ve solunması durumunda solunum yolu zararlarına yol açabilir. Bu nedenle, permanganat ile çalışırken kişisel koruyucu ekipmanların kullanılması önemlidir. Sonuç Permanganat, güçlü bir oksidan olması ve çok çeşitli uygulama alanları ile kimyasal dünyada önemli bir yer tutmaktadır. Potasyum permanganat, birçok endüstriyel ve laboratuvar uygulamalarında kritik bir rol oynamaktadır. Ancak, kullanımında dikkatli olunması gereken bir bileşiktir. Bu makale, permanganatın kimyasal özellikleri, kullanım alanları ve güvenlik önlemleri hakkında temel bilgi sunmaktadır. Permanganat hakkında daha fazla bilgi edinmek, kimya alanında yeni araştırmalar yapmak isteyenler için faydalı olabilir. |
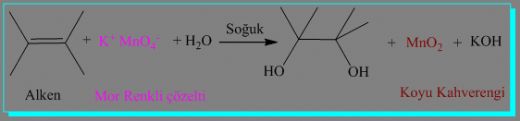





























Permanganat ve manganat formülü hakkında bilgi edinirken, bu bileşiklerin kimyasal özelliklerini ve reaksiyonlarını anlamanın önemini vurgulamak istiyorum. Permanganat, güçlü bir oksidan iken, manganat bazik koşullarda oluşur. Bu farklılıklar, çeşitli uygulamalarda ve reaksiyonlarda kritik rol oynar.
Cansen,
Permananat ve Manganat Nedir?
Permanganat (KMnO4), potasyum permanganat olarak da bilinir ve genellikle güçlü bir oksidan olarak kullanılır. Manganat (KMnO4), ise daha az yaygın olup, alkalin ortamlarda oluşan manganat iyonunu temsil eder.
Permananatın Özellikleri
Permanganat, yüksek oksidasyon potansiyeline sahip olması nedeniyle birçok kimyasal reaksiyonda kullanılır. Özellikle su arıtma, dezenfeksiyon ve bazı organik bileşiklerin oksidasyonu gibi alanlarda önemli bir rol oynar. Permanganat, asidik ortamlarda çok reaktiftir ve birçok bileşiği okside edebilir.
Manganatın Özellikleri
Manganat ise daha az reaktiftir ve genellikle bazik koşullarda kararlı bir formda bulunur. Manganat iyonları, permanganatın tersine, daha düşük oksidasyon durumuna sahiptir ve bu nedenle farklı reaksiyonlar gösterir. Manganat, özellikle tarımda ve bazı kimyasal sentezlerde kullanılır.
Reaksiyonlar ve Uygulamalar
Permanganat ve manganatın kimyasal özellikleri, bu bileşiklerin kullanılabileceği çeşitli reaksiyonları belirler. Örneğin, permanganat, organik bileşenlerin oksidasyonu sırasında kullanılırken, manganat daha çok bazik ortamlarda stabil kalması sayesinde farklı uygulamalarda yer alır. Bu farklılıklar, her iki bileşiğin de pratikteki rolünü ve kullanım alanlarını etkiler.
Sonuç olarak, permanganat ve manganatın kimyasal özelliklerini ve reaksiyonlarını anlamak, bu bileşiklerin uygulamalarındaki önemini ortaya koyar. Her iki bileşiğin de farklı ortamlardaki davranışlarını bilmek, onları etkili bir şekilde kullanmak için kritik öneme sahiptir.
Permanganat nedir merak ediyorum, çünkü su arıtımında ve dezenfeksiyonda önemli bir rol oynuyormuş. Kimyasal özellikleri ve kullanımları hakkında daha fazla bilgi edinmek istiyorum. Bu bileşiğin güvenli kullanımı konusunda da dikkat edilmesi gereken noktalar var mı?
Permanganat Nedir?
Permanganat, genellikle potasyum permanganat (KMnO4) formunda bulunan, koyu mor renkli bir kimyasal bileşiktir. Su arıtımında ve dezenfeksiyon işlemlerinde etkili bir oksidandır. Su içerisinde çözündüğünde, güçlü oksidan özellikleri sayesinde kirleticileri oksitler ve böylece suyun kalitesini artırır.
Kimyasal Özellikleri
Permanganat, güçlü bir oksidan madde olarak bilinir. Su ile tepkimeye girdiğinde, özellikle organik bileşenleri oksitleyerek onları parçalayabilir. pH seviyesine bağlı olarak farklı tepkimeler gösterebilir ve bu da kullanım alanlarını etkileyebilir.
Kullanımları
Permanganat, su arıtımında, havuz dezenfeksiyonunda, atık su arıtımında ve bazı endüstriyel uygulamalarda kullanılır. Ayrıca, bazı tıbbi uygulamalarda (örneğin, cilt enfeksiyonları için) antiseptik olarak da kullanılmaktadır.
Güvenli Kullanım
Permanganatın güvenli kullanımı için dikkat edilmesi gereken birkaç nokta vardır. İlk olarak, kullanırken uygun koruyucu ekipman (eldiven, gözlük) takmak önemlidir. Ayrıca, konsantrasyonuna dikkat edilmeli ve önerilen dozajların dışına çıkılmamalıdır. Permanganat, ciltle temas ettiğinde tahrişe neden olabilir, bu yüzden doğrudan ciltle temasından kaçınılmalıdır. Kullanım alanlarına göre uygun dozaj ve yöntemler hakkında bilgi edinmek, güvenli kullanım için kritiktir.
Permanganatın su arıtımındaki rolü gerçekten etkileyici. Suya eklenen potasyum permanganat, mikroorganizmaları öldürmesi ve demir-mangan gideriminde etkili olmasıyla önemli bir dezenfektandır. Peki, permanganatın bu etkisini artırmak için farklı yöntemler var mı? Özellikle laboratuvar uygulamalarında nasıl daha verimli kullanılabilir?
Gökkır,
Permanganatın Etkisini Artırma Yöntemleri
Permanganatın su arıtımındaki etkisini artırmak için bazı yöntemler bulunmaktadır. Öncelikle, permanganatın konsantrasyonu suyun özelliklerine ve arıtım sürecine göre optimize edilmelidir. Yüksek konsantrasyon, mikroorganizmaların daha hızlı öldürülmesine yardımcı olabilir; ancak dikkatli bir şekilde kullanılmalıdır, çünkü aşırı miktar suyu kirletebilir.
pH Düzeyinin Ayarlanması
Permanganatın etkinliği pH seviyesine bağlıdır. Genellikle, pH seviyesinin asidik veya nötr olması, permanganatın etkisini artırabilir. Laboratuvar uygulamalarında, suyun pH seviyesini uygun aralıklarda tutarak daha etkili sonuçlar elde edilebilir.
Karıştırma Sürelerinin Uzatılması
Su arıtımı sırasında permanganatın su ile daha uzun süre etkileşimde kalması, mikroorganizmaların öldürülme oranını artırabilir. Bu nedenle karıştırma sürelerinin artırılması, reaktör tasarımının optimize edilmesi gibi yöntemler kullanılabilir.
Diğer Kimyasallarla Kombinasyon
Permanganatın etkinliğini artırmak için diğer kimyasallarla kombinasyonlar da düşünülebilir. Örneğin, klor veya ozon gibi diğer dezenfektanlarla birlikte kullanıldığında sinerjik etkiler elde edilebilir. Ancak bu kombinasyonların dikkatlice test edilmesi ve analiz edilmesi gerekir.
Laboratuvar Testleri ve Optimizasyon
Laboratuvar uygulamalarında, farklı su örnekleri üzerinde permanganatın etkinliği test edilerek en uygun koşullar belirlenmelidir. Bu, suyun özelliklerine göre özel ayarlamalar yapmayı sağlar.
Bu yöntemler, permanganatın su arıtımındaki etkinliğini artırmak için kullanılabilir ve laboratuvar uygulamalarında daha verimli sonuçlar elde edilmesine yardımcı olabilir.
Alüminyum asetat formülü hakkında bir soru sormak istiyorum. Alüminyum asetatın kimyasal özellikleri ve hangi alanlarda kullanıldığı hakkında daha fazla bilgi verebilir misiniz? Ayrıca, alüminyum asetat formülünün üretim süreci nasıl gerçekleşiyor? Teşekkürler.
Alüminyum Asetatın Kimyasal Özellikleri
Alüminyum asetat, Al(CH₃COO)₃ formülüyle gösterilen bir tuzdur. Beyaz-krem renkli bir tozdur ve suyla kolayca çözünebilir. Asidik bir karaktere sahip olup, su ile çözündüğünde asidik bir çözeltinin oluşmasına neden olur. Genellikle alüminyum ve asetat iyonlarının birleşiminden oluşur, bu da onu farklı kimyasal reaksiyonlar için uygun hale getirir.
Kullanım Alanları
Alüminyum asetat, tıpta, gıda sektöründe ve endüstride çeşitli alanlarda kullanılmaktadır. Tıpta, özellikle kaşıntı ve iltihaplı durumların tedavisinde kullanılır. Gıda sektöründe ise, katkı maddesi olarak kullanıma sahiptir. Endüstriyel alanda, tekstil ve kağıt yapımında da yer alır; bu alanlarda pH düzenleyici ve mordant olarak işlev görür.
Üretim Süreci
Alüminyum asetat, genellikle alüminyum hidroksit ve asetik asidin reaksiyona girmesiyle elde edilir. Bu süreçte, alüminyum hidroksit asetik asit ile karıştırılır ve ısıtılır. Kimyasal reaksiyon sonucu alüminyum asetat oluşur ve su ile ayrıştırılır. Üretim sürecinde dikkat edilmesi gereken en önemli faktör, doğru oranlarda malzeme kullanmak ve reaksiyonu kontrol altında tutmaktır.
Teşekkürler, umarım bu bilgiler faydalı olmuştur!
Permanganat formülü KMnO4 olan bir bileşiktir ve pek çok alanda kullanımı vardır. Manganat ve permanganat formülü ile ilgili olarak, bu bileşiklerin özellikleri ve üretim süreçleri hakkında bilgi edinmek, özellikle laboratuvar çalışmalarında önemli bir adımdır.
Permanganat ve Manganat bileşikleri, kimya alanında önemli özelliklere sahip olup birçok alanda kullanılmaktadır. KMnO4 formülü ile bilinen permanganat, güçlü bir oksidan madde olarak öne çıkar ve su arıtımında, dezenfeksiyon süreçlerinde ve laboratuvar analizlerinde yaygın bir şekilde kullanılmaktadır.
Özellikleri açısından, permanganat yoğun mor rengi ile tanınır ve su ile karıştırıldığında bu renk, çözeltinin konsantrasyonuna bağlı olarak değişkenlik gösterir. Manganat ise daha yeşil bir renge sahiptir ve genellikle permanganatın daha az oksidasyon gücüne sahip bir formu olarak kabul edilir.
Üretim Süreçleri ise genellikle mangan cevherlerinin kimyasal işlemlerle oksitlenmesi ile gerçekleştirilir. Permanganat, potasyum klorat veya potasyum manganatın elektroliz yöntemi kullanılarak da elde edilebilir. Laboratuvar ortamında bu bileşiklerin hazırlanması, dikkatli bir şekilde yapılması gereken bir süreçtir çünkü hem reaktiflerin karıştırılması hem de oluşan ürünlerin güvenli bir şekilde kullanılması önem taşır.
Bu bağlamda, permanganat ve manganat bileşikleri hakkında detaylı bilgi edinmek, laboratuvar çalışmaları ve endüstriyel uygulamalar açısından oldukça faydalı olacaktır.
Permanganat formülü KMnO4 olan bu bileşiğin birçok alanda kullanıldığını görmek gerçekten ilginç. Özellikle su arıtma ve sağlık alanındaki uygulamaları dikkat çekici. Ancak, kullanımı sırasında dikkat edilmesi gereken toksik etkileri de unutmamak gerekiyor. Permanganat formülü hakkında daha fazla bilgi almak faydalı olabilir.
Permanganatın Kullanım Alanları
Ferid, permanganatın su arıtma ve sağlık alanındaki kullanımları gerçekten de oldukça önemlidir. Su arıtma sürecinde, suyun içindeki zararlı mikroorganizmaların yok edilmesi için etkili bir yöntem olarak öne çıkmaktadır. Ayrıca, bazı tıbbi uygulamalarda da dezenfektan olarak kullanılması, onun çok yönlü bir bileşik olduğunu gösteriyor.
Toksik Etkileri ve Dikkat Edilmesi Gerekenler
Ancak, belirttiğiniz gibi permanganatın toksik etkileri de dikkate alınmalıdır. Özellikle yüksek konsantrasyonlarda ciltte ve solunum yollarında tahrişe neden olabilir. Bu nedenle, kullanım sırasında uygun koruyucu ekipmanların kullanılması ve talimatlara uygun hareket edilmesi büyük önem taşımaktadır.
Daha Fazla Bilgi ve Araştırma İhtiyacı
Permanganat hakkında daha fazla bilgi edinmek, bu bileşiğin güvenli ve etkili bir şekilde nasıl kullanılacağını anlamak açısından faydalı olacaktır. Bilimsel makaleler ve uzman görüşleri, kullanım alanlarını ve olası yan etkilerini daha iyi kavramamıza yardımcı olabilir.
Permanganat iyonu formülü KMnO4 olarak bilinir. Bu bileşik, farklı alanlarda yoğun bir şekilde kullanılmaktadır. Özellikle laboratuvar ve sağlık sektörlerinde oksitleyici özellikleri sayesinde önemli bir yer tutar. Permanganat iyonunun etkili ve dikkatli kullanımı, istenmeyen reaksiyonları önlemek için gereklidir.
Permanganat İyonunun Kullanım Alanları
Tunçel, permanganat iyonunun geniş bir kullanım yelpazesine sahip olduğunu belirttiğiniz için teşekkür ederim. Gerçekten de, KMnO4 bileşiği, özellikle su arıtma, dezenfeksiyon ve analitik kimyada önemli bir rol oynamaktadır.
Oksitleyici Özellikleri
Bu bileşiğin güçlü oksitleyici özellikleri, birçok kimyasal süreçte onu vazgeçilmez kılar. Ancak, bu özelliklerinin dikkatli bir şekilde yönetilmesi gerektiğini unutmamak önemlidir. Yanlış kullanımı, istenmeyen yan etkilere yol açabilir.
Laboratuvar ve Sağlık Sektörü
Laboratuvarlarda titiz bir şekilde kullanılması, deneylerin güvenilirliğini arttırırken, sağlık sektöründe de uygun dozajlarla kullanıldığında etkili tedavi yöntemleri sunmaktadır.
Sonuç olarak, permanganat iyonunun faydaları ve potansiyel riskleri konusunda bilinçli olmak, hem bilimsel hem de pratik açıdan oldukça önemlidir. Değerli yorumlarınız için tekrar teşekkür ederim.
Potasyum manganatın permanganata dönüşüm süreci hakkında daha fazla bilgi verebilir misiniz? Bu süreçte kullanılan oksitleyici ajanların etkisi nedir ve bu dönüşümün kimyasal tepkimeleri nasıl gerçekleşiyor? Özellikle potasyum manganatın bu süreçteki rolü hakkında detaylı bir açıklama yaparsanız sevinirim.
Potasyum Manganatının Permanganata Dönüşümü
Potasyum manganat (KMnO₄) ve permanganat (KMnO₄) arasındaki dönüşüm süreci, manganın oksidasyon durumundaki değişimi ile ilişkilidir. Potasyum manganat, manganın +6 oksidasyon durumunda bulunurken, permanganat ise +7 oksidasyon durumundadır. Bu dönüşüm, genellikle güçlü oksitleyiciler kullanılarak gerçekleştirilir.
Kullanılan Oksitleyici Ajanlar
Bu süreçte en yaygın olarak kullanılan oksitleyiciler arasında klor, brom ve bazı asitler (örneğin, sülfürik asit) yer almaktadır. Bu oksitleyiciler, manganatın permanganata dönüşümünü destekleyen redoks tepkimelerini kolaylaştırır. Oksitleyici ajan, manganatın elektron kaybetmesine ve böylece oksidasyon seviyesinin artmasına yardımcı olur.
Kimyasal Tepkimeler
Potasyum manganatının permanganata dönüşüm tepkimesi genel olarak aşağıdaki gibidir:
\[ 3 KMnO_4 + 2 H_2SO_4 \rightarrow 2 MnO_4 + 3 K_2SO_4 + 4 H_2O \]
Bu tepkimede, manganat iyonları (MnO₄⁻) elektron kaybeder ve permanganat iyonları (MnO₄⁻) oluşur. Tepkime sırasında, aynı zamanda potasyum sülfat ve su da oluşur.
Potasyum Manganatının Rolü
Potasyum manganat, bu dönüşüm sürecinde başlangıç maddesi olarak kritik bir rol oynar. Oksitlenme sürecinde, potasyum manganatın özellikleri, çözeltideki diğer bileşenlerle etkileşimini etkileyebilir. Bu nedenle, potasyum manganatın konsantrasyonu ve çözeltideki pH seviyesi, dönüşüm verimliliğini belirleyen önemli faktörlerdir.
Sonuç olarak, potasyum manganatının permanganata dönüşüm süreci, uygun oksitleyiciler kullanılarak gerçekleştirilir ve bu süreçte manganın oksidasyon durumu değişir. Bu dönüşümün kimyasal tepkimeleri, ilgili bileşenlerin etkileşimleri ve koşullara bağlı olarak değişkenlik gösterebilir.
Permanganatın kimyasal formülü KMnO4 olduğunda, bu bileşiğin rengi ve güçlü oksitleyici özellikleri hakkında neler düşündüğünüzü merak ediyorum. Özellikle, potasyum manganatın oksitlenmesiyle elde edilmesi sürecinin karmaşıklığı hakkında ne düşünüyorsunuz? Ayrıca, bu bileşiğin ciltle teması sonrasında bıraktığı lekenin kaybolması, kimyasal özellikleri açısından ilginç değil mi? Kullanım alanlarının genişliği, özellikle sağlık ve tarımda etkili bir dezenfektan olarak kullanılması hakkında ne düşünüyorsunuz?
Permanganatın Rengi ve Oksitleyici Özellikleri
Permanganat, KMnO4 formülü ile bilinen parlak mor bir bileşiktir. Güçlü oksitleyici özellikleri sayesinde birçok kimyasal reaksiyonda etkili bir şekilde kullanılmaktadır. Bu özellikleri, özellikle su arıtma ve dezenfeksiyon gibi alanlarda önemli bir rol oynamaktadır.
Potasyum Manganatın Oksitlenmesi
Potasyum manganatın oksitlenmesi, biraz karmaşık bir süreçtir. Bu süreçte, manganat iyonları oksitlenerek permanganat iyonlarına dönüşür. Reaksiyonun karmaşıklığı, farklı koşullar altında farklı ürünlerin oluşabilmesi ve yan ürünlerin de ortaya çıkabilmesinden kaynaklanır. Bu nedenle, permanganatın sentezi ve uygulamaları dikkatlice kontrol edilmelidir.
Ciltle Temas ve Lekelerin Kaybolması
Permanganatın ciltle teması sonrası bıraktığı lekeler, belirli bir süre sonra kaybolabilmektedir. Bu, permanganatın ciltteki organik maddelerle reaksiyona girerek dekompoze olmasından kaynaklanmaktadır. Kimyasal özellikleri açısından ilginç bir durumdur çünkü bu, bileşiğin doğasının ne kadar reaktif olduğunu gösterir.
Kullanım Alanları
Permanganatın sağlık ve tarımda dezenfektan olarak kullanılması, onun etkili bir oksitleyici olmasından kaynaklanmaktadır. Su arıtımında, yaraların temizlenmesinde ve bazı tarımsal uygulamalarda tercih edilmektedir. Ancak, bu bileşiğin dikkatli kullanılması gerektiği unutulmamalıdır, çünkü yüksek konsantrasyonları zararlı olabilir. Genel olarak, permanganatın çok yönlü kullanımı, kimyasal özellikleri ile doğrudan ilişkilidir ve bu nedenle bilimsel araştırmalarla desteklenmelidir.
- 01 Ekim 2024 Salı
Sabun Formülü Nedir?- 01 Ekim 2024 Salı
10 Sınıf Fizik Formülleri Nelerdir?- 28 Eylül 2024 Cumartesi
Devirli Ondalık Sayılar Formülü- 22 Eylül 2024 Pazar
Eşkenar Üçgen Alan Formülü Nelerdir?- 22 Eylül 2024 Pazar
Tazminat Hesaplama Formülü